Физика
При рассмотрении идеального газа, находящегося в открытом сосуде, необходимо учитывать, что вследствие изменения термодинамических параметров часть газа выходит из сосуда. При этом уравнение состояния записывается только для той части газа, которая остается в сосуде.
Для идеального газа, находящегося в открытом сосуде, необходимо учитывать следующее:
- масса газа изменяется в результате изменения его термодинамических параметров:
m ≠ const;
- рассматривается газ, оставшийся в сосуде определенного объема, т.е. объем газа фиксирован:
V = const;
- давление газа может изменяться или оставаться постоянным (в зависимости от условия задачи), причем на изменение давления в условии задачи обычно бывает четкое указание.
Если давление идеального газа в открытом сосуде по условию задачи изменяется (p ≠ const), то уравнение Менделеева — Клапейрона записывается для двух состояний газа в виде системы (рис. 5.7):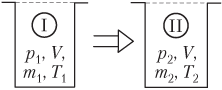
где p 1, m 1, T 1 — давление, масса и температура газа в начальном состоянии; p 2, m 2, T 2 — указанные параметры газа в конечном состоянии; V — объем сосуда; M — молярная масса газа; R — универсальная газовая постоянная, R ≈ 8,31 Дж/(моль ⋅ К).
Если давление идеального газа в открытом сосуде по условию задачи остается постоянным (p = const), то изменения некоторых характеристик газа в открытом сосуде можно вычислить по следующим формулам:
- изменение массы
,
где m 1 — первоначальная масса газа; m 2 — масса газа в конце процесса; T 1 — термодинамическая (абсолютная) температура газа в начале процесса; T 2 — термодинамическая (абсолютная) температура газа в конце процесса;
- изменение плотности
,
где ρ1 — первоначальная плотность газа; ρ2 — плотность газа в конце процесса;
- изменение количества вещества
,
где ν1 — первоначальное количество вещества (газа) в сосуде; ν2 — количество вещества (газа) в сосуде в конце процесса.
Пример 11. В открытом сосуде объемом 450 дм3 содержится некоторое количество идеального газа. Температуру газа увеличивают от 27 до 177 °С. Давление газа остается постоянным и равным 166 кПа. Сколько моль газа выйдет из сосуда?
Решение. Запишем уравнение Менделеева — Клапейрона для двух состояний газа, находящегося в открытом сосуде, при нагревании:
- для начального состояния
pV = ν1RT 1;
- для конечного состояния
pV = ν2RT 2;
где p — давление газа, p = const; V — объем газа (сосуда), V = const; ν1, ν2 — количество вещества (газа) в начале и в конце процесса; R — универсальная газовая постоянная, R = 8,31 Дж/(моль ⋅ К); T 1, T 2 — температура газа в начале и в конце процесса.
Первое уравнение позволяет получить формулу для расчета количества вещества (газа) в начале процесса:
.
Подстановка полученной формулы в уравнение
дает искомую разность
.
Для вычисления искомой величины необходимо перевести температуру из градусов Цельсия в кельвины:
T 1 = t 1 + 273 = 27 + 273 = 300 К,
T 2 = t 2 + 273 = 177 + 273 = 450 К.
Произведем вычисление:
моль.
При нагревании из сосуда вышло 10 моль газа.
Пример 12. В баллоне при температуре 15 °С находится идеальный газ. Из баллона выходит 40 % газа, а температура при этом понижается на 8,0 °С. Во сколько раз уменьшится давление газа в баллоне?
Решение. Запишем уравнение Менделеева — Клапейрона для двух состояний газа, находящегося в открытом сосуде:
- для начального состояния
p 1V = ν1RT 1;
- для конечного состояния
p 2V = ν2RT 2;
где p 1 — давление газа в начальном состоянии; p 2 — давление газа в конечном состоянии; V — объем газа (сосуда), V = const; ν1, ν2 — количество вещества (газа) в начале и в конце процесса соответственно; R — универсальная газовая постоянная, R = 8,31 Дж/(моль ⋅ К); T 1, T 2 — температура газа в начале и в конце процесса соответственно.
Искомой величиной является отношение давлений p 1/p 2, которое определим из отношения уравнений:
, т.е. .
В результате процесса из баллона выходит 40 % газа, поэтому количество вещества (газа) ν2, оставшегося в баллоне, составляет 60 % от количества вещества (газа) ν1, которое было в начале процесса:
ν2 = 0,6ν1.
Для вычисления искомой величины необходимо сделать перевод температуры, заданной в градусах Цельсия, в кельвины:
T 1 = t 1 + 273 = 15 + 273 = 288 К,
T 2 = t 2 + 273 = (t 1 − Δt) + 273 = (15 − 8,0) + 273 = 280 К.
Подстановка температур и количества вещества (газа), оставшегося в баллоне, в выражение для искомой величины дает
.
Давление газа в баллоне понизится в 1,7 раза.










