Химия
Химия — наука о веществах, их строении, свойствах и превращениях.
В самом широком смысле вещество — это то, из чего состоят физические тела. Например, физическое тело «железный гвоздь» состоит из вещества железо. Физическое тело может состоять как из одного вещества (физическое тело «медная проволока» состоит из одного вещества — меди), так и из нескольких (физическое тело «автомобиль» состоит из различных металлов, пластмасс). Одно и то же вещество, в свою очередь, может образовывать несколько физических тел. Например: вещество вода образует айсберги, капли дождя, снежинки, иней; только из вещества железо состоят железные гвоздь, скрепка, проволока. В отличие от физического тела, понятие «вещество» абстрактное, вещество нельзя потрогать, нарисовать.
Вещество — только одна из форм материи. Вторая форма существования материи — поле. Поле — это материальная среда, посредством которой тела или частицы вещества взаимодействуют между собой. Примеры полей: гравитационное, электрическое, магнитное, ядерные силы. Вещество имеет дискретное (прерывистое, корпускулярное) строение, поскольку состоит из атомов, а поле однородно, непрерывно. Частицы поля (кванты), в отличие от частиц вещества, не имеют массы покоя (это означает, что они всегда находятся в движении). Характеристики поля: частота, потенциал, напряженность. Характеристики вещества: масса (покоя), размеры, плотность, окраска и т.д.
Традиционно физика и химия понятие «вещество» рассматривают по-разному. В физическом смысле веществом являются все материальные объекты, имеющие массу покоя; иными словами, это не только, например, порция воды массой 1 г, но и отдельно взятая молекула воды, а также любая элементарная частица — электрон, протон или нейтрон.
С химической точки зрения вещество — это устойчивая совокупность атомов, молекул или ионов:
- находящаяся в определенном агрегатном состоянии,
- обладающая некоторым набором постоянных при данных условиях физических и химических свойств.
Пример 1.1. Укажите химические вещества: а) молекула воды; б) порция аммиака массой 10 г; в) соляная кислота; г) медный таз; д) порция метана объемом 1,12 дм3.
1) б, в, г, д; 3) а, б, в, д;2) б, в, д; 4) б, д.Решение. Молекула воды является веществом только в физическом смысле, так как имеет массу, но не имеет определенного агрегатного состояния. Соляная кислота — это не вещество, а смесь HCl и H2O, медный таз — физическое тело. О веществах в химическом смысле говорится в случаях б), д).
Ответ: 4).
Физические свойства вещества — это набор определенных констант, характеризующих его агрегатное состояние, плотность, температуры плавления и кипения, цвет, растворимость, твердость, вязкость, летучесть, запах и вкус, теплопроводность, электрическую проводимость, магнитные и оптические свойства, диэлектрическую проницаемость и т.д.
Химические свойства вещества — это совокупность данных о том, с какими веществами и при каких условиях реагирует данное вещество и в какие другие вещества оно при этом превращается.
Например, физические свойства воды: бесцветная жидкость (обычные условия), без цвета, запаха и вкуса, плотность (н.у.) равна 1 г/см3, температуры кипения и плавления соответственно 100 °С и 0 °С, плохо проводит электрический ток. Химические свойства воды: взаимодействует с кислотными и основными оксидами, некоторыми металлами, при электролизе разлагается на водород и кислород.
Свойства вещества зависят от его состава и строения. Различают качественный и количественный состав вещества.
Качественный состав — это природа атомов, образующих вещество. Количественный состав — это число атомов каждого элемента в составе молекулы или в формульной единице вещества.
Например, вещество гидроксид натрия состоит из атомов натрия, кислорода и водорода (качественный состав), причем в формульной единице вещества, NaOH, мольное отношение атомов равно 1:1:1 (количественный состав).
Под строением вещества понимается природа его структурных единиц (молекулы — в случае веществ молекулярного строения или формульные единицы — для веществ немолекулярного строения), взаимное положение атомов и структурных единиц, длины связей, валентные углы, распределение электронной плотности в молекуле или формульной единице. Например, именно о строении идет речь, когда мы говорим, что вещество вода состоит из молекул, молекулы воды имеют угловое строение (валентный угол равен 105°), связь в молекуле ковалентная полярная.
Каждое вещество имеет свое название (названия). Названия бывают:
- международные (систематические): NaCl — хлорид натрия; KNO3 — нитрат калия; H2SO4 — сульфат водорода;
- традиционные (привычные): H2SO4 — серная кислота; H3PO4 — фосфорная кислота;
- специальные: NH3 — аммиак; H2O — вода; H2S — сероводород;
- тривиальные: олеум, норвежская селитра, угарный газ, пирит, галит, сусальное золото.
В зависимости от качественного состава вещества делят на простые и сложные. Простые вещества состоят из атомов одного элемента, причем число атомов в структурной единице простого вещества может быть разным: аргон Ar, медь Cu, водород Н2, кислород О2, белый фосфор Р4, ромбическая сера S8. Сложные вещества (химические соединения) состоят из атомов различных элементов. Например, вода Н2О, аммиак NH3, метан CH4. Сложные вещества, в отличие от простых, можно разложить на несколько других простых и/или сложных веществ:
2H2O 2H2↑ + O2↑
2KNO3 2KNO2 + O2↑
CaCO3 CaO + CO2↑
В свою очередь простые вещества делятся на неметаллы и металлы. Неметаллы, как правило, плохо проводят теплоту и электрический ток, при обычных условиях могут быть жидкими (бром), твердыми (кремний, бор, сера) или газообразными (водород, кислород, азот, хлор). Металлы (медь, железо, кальций) хорошо проводят электрический ток и теплоту, твердые при обычных условиях (кроме ртути), ковкие, непрозрачные.
Сложные вещества классифицируются:
- по происхождению (органические и неорганические);
- составу (бинарные, т.е. состоящие из атомов двух различных элементов — CaO, H2O, PH3, и многоэлементные, состоящие из атомов трех и более различных элементов — H3PO4, CH3COOH).
Бинарные вещества в свою очередь делятся на оксиды (CuO, K2O), нитриды (Ca3N2), фосфиды (Mg3P2), карбиды (CaC2), гидриды (NaH), галогениды (KCl, FeBr3) и халькогениды (K2S, CS2, Al2Se3).
Среди многоэлементных веществ различают соли, гидроксиды (кислородсодержащие кислоты, основания и амфотерные гидроксиды), комплексные соединения (K3[Al(OH)6], Na2[Zn(OH)4]) и кристаллогидраты (CuSO4 ⋅ 5H2O, Na2SO4 ⋅ 7H2O). Комплексные соединения содержат внешнюю и внутреннюю (указана в квадратных скобках) сферы. Частицы, образующие внутреннюю сферу соединения, очень устойчивы и в водных растворах существуют самостоятельно: [Al(OH)6]3−, [Zn(OH)4]2−.
При записи формул бинарных соединений вначале, как правило, записывается символ менее электроотрицательного элемента. Исключения: аммиак NH3, гидразин N2H4, углеводороды CH4, C2H2 и др., фосфин PH3.
Физические и химические явления
В природе с веществами происходят различные изменения (явления), которые принято классифицировать на химические и физические.
Физические явления — это изменения агрегатного состояния, скорости движения, температуры и формы тел. При этих явлениях новые вещества не образуются. Например, таяние снега, испарение воды, возгонка (сублимация) сухого льда СО2 (сублимация — переход вещества при нагревании из твердого состояния в газообразное, минуя жидкое).
К физическим явлениям относятся также ядерные реакции:
и радиоактивные превращения:
В этих процессах новые вещества хотя и образуются, однако это связано с изменением природы атомов.
Химические явления, или химические реакции — это изменения веществ, процесс их превращения в другие вещества, протекающий без изменения природы атомов (атомы в химических реакциях сохраняются).
В результате химических явлений могут изменяться:
- как качественный состав, так и строение веществ:
BaCl2 + H2SO4 = BaSO4 + 2HCl
- только строение веществ с сохранением качественного и количественного состава:
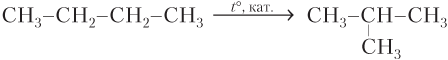
CH3–CH2–CH=CH2 CH3–CH=CH–CH3
C (алмаз) C (графит);
- количественный состав (с сохранением качественного) и строение:
3O2 = 2O3
2NO → N2O4
1. В результате химических явлений молекулы (формульные единицы) разрушаются, а атомы не изменяются (сохраняются).
2. Ядерные реакции и радиоактивные превращения относятся к физическим явлениям.
Каждому химическому явлению сопутствует физическое, которое может быть зафиксировано непосредственно нашими органами чувств или специальными приборами. К числу важнейших физических признаков химических явлений относятся выделение газа, выпадение или растворение осадка, изменение окраски, выделение или поглощение теплоты, излучение света, появление запаха.
Следует иметь в виду, что само по себе каждое из отмеченных физических явлений еще не будет однозначным признаком химической реакции. Например, если ударить молотком по куску железа, то выделится тепло и железо нагреется (механическая энергия переходит в тепловую), однако новые вещества при этом не образуются. Откроем флакон с духами — появится запах, но и в этом случае новые вещества не образуются. Оба описанных явления относятся к физическим. Однозначный признак химической реакции — это образование новых веществ.
Закон сохранения массы вещества
Поскольку при химических реакциях атомы не исчезают и их природа сохраняется (новые атомы не образуются), то и общее число атомов до и после реакции остается неизменным. Отсюда следует закон сохранения массы в химических реакциях (М.В. Ломоносов, 1748; А. Лавуазье, 1789): масса веществ, вступивших в химическую реакцию, равна массе продуктов.
Отметим, что этот закон справедлив только в практическом смысле, так как из-за взаимосвязи массы и энергии выделение или поглощение теплоты (энергии) в химических реакциях должно приводить к тому, что массы исходных веществ и продуктов будут различаться. Оценим численное значение этого различия.
Связь массы и энергии выражается уравнением А. Эйнштейна:
Е = mc 2,
где c — скорость света (c = 3 ⋅ 108 м/с).
Отсюда следует, что изменение массы
.
Для химических реакций значение ΔЕ(Q) порядка нескольких сотен килоджоулей, поэтому при огромной скорости света значения Δm получаются чрезвычайно малыми (≈ 10−9 г) и не поддаются непосредственному измерению. (Изменение энергии огромно в ядерных реакциях, например процессах образования ядер атомов из протонов и нейтронов. Это приводит к так называемому дефекту масс, суть которого состоит в том, что масса ядра атома всегда меньше общей суммы масс составляющих его протонов и нейтронов.) Тем не менее, более правильно говорить о сохранении не только массы, но и энергии (т.е. материи) в химических реакциях:
суммарные масса и энергия веществ, вступающих в химическую реакцию, равны суммарным массам и энергии продуктов реакции.
Чистые вещества и смеси
В природе вещества встречаются как в индивидуальном виде (так называемые чистые вещества), так и (чаще) в виде смесей.
Смесь — система, состоящая из двух и более разных веществ, не изменяющих свои свойства в результате смешивания. Примеры смесей: молоко, бетон, дым, туман, пена.
1. Абсолютно чистых веществ в природе нет и быть не может.
2. Смеси к веществам не относятся.
Вещество считают чистым (индивидуальным), если содержание примесей в нем настолько мало, что практически не влияет на физические и химические свойства вещества.
Чистые сложные вещества следует отличать от смесей (табл. 1.1).
| Сложное вещество | Смесь веществ |
|---|---|
| Образуется в результате химической реакции | Образуется при смешивании |
| Физические и химические свойства отдельных веществ, из которых получено сложное вещество, не сохраняются | Физические и химические свойства веществ, образующих смесь, сохраняются (исключение — растворы) |
| Имеет определенный качественный и количественный состав, который может быть выражен химической формулой | Состав произвольный и не может выражаться определенной химической формулой |
| Разлагается на составные части только в химических реакциях | Можно разделить на составные компоненты сравнительно простыми физическими методами (выпаривание, фильтрование и т.д.) |
| Физические свойства постоянные | Физические свойства не постоянные |
Например, при нагревании железных опилок с серой образуется новое химическое вещество с определенным качественным и количественным составом — сульфид железа(II) FeS. В составе FeS химические свойства веществ железо и сера утрачены, не проявляются. Разложить сульфид железа(II) на отдельные простые вещества железо и серу простыми физическими методами нельзя. Плотность сульфида железа(II) постоянна, магнитом это вещество не притягивается.
Смешаем железные опилки и серу без нагревания. Во-первых, смешивать эти вещества можно в любых соотношениях (состав смеси произвольный и не имеет определенной формулы), во-вторых, железо и сера не утратили своих свойств (в составе смеси железо так же притягивается магнитом, как и индивидуальное железо); эту смесь можно разделить на отдельные компоненты с помощью магнита или воды (сера водой не смачивается и остается на ее поверхности), ее плотность не постоянна и возрастает с увеличением содержания железа.
Смеси делятся на однородные и неоднородные. В однородных (гомогенных) смесях отдельные компоненты нельзя различить не только невооруженным глазом, но и с помощью микроскопа. Однородными смесями являются растворы. В неоднородных (гетерогенных) смесях отдельные компоненты можно различить невооруженным глазом (смесь бензина и воды) или с помощью микроскопа (сливки). Неоднородные смеси часто называются механическими.
Из неоднородных смесей отдельные компоненты выделяют:
- отстаиванием (смесь воды и подсолнечного масла, воды и глины);
- фильтрованием (смесь воды и глины, воды и осадка BaSO4);
- с помощью магнита (смесь железных и древесных опилок, железа и серы).
Однородную смесь разделяют на отдельные вещества:
- выпариванием (смесь NaCl и H2O),
- дистилляцией (перегонкой); этот метод основан на различии температур кипения компонентов.
Примеры разделения однородных смесей методом перегонки:
а) нефть представляет собой смесь различных углеводородов. При постепенном нагревании нефти происходит ее разделение на отдельные фракции (процесс называется ректификацией) со все большей молярной массой углеводородов;
б) для получения азота и кислорода из воздуха последний предварительно повышением давления и понижением температуры переводят в жидкое состояние. Затем полученную жидкую смесь нагревают, вначале испаряется азот (его молекулы более легкие), оставшаяся жидкость представляет собой чистый кислород.
Примеры неоднородных смесей: томатный сок, шоколад, взвесь глины в воде, смесь железных и древесных опилок.
Примеры однородных смесей: нашатырный спирт — смесь NH3 и H2O; соляная кислота — смесь HCl и H2O; раствор этанола в воде.










